
Włoskie wskazówki dot. opieki nad pacjentem w stanie krytycznym
Włoskie wskazówki dot. opieki nad pacjentem w stanie krytycznym
Około 5% pacjentów zarażonych przez COVID-19 może być w stanie klinicznym wymagającym hospitalizacji na intensywnej terapii, z koniecznością wspomagania oddychania.
Uważa się więc za konieczne, by Regiony przygotowały plan kryzysowy względem pacjentów w stanie krytycznym, chorych na COVID 19, pozwalający na zapewnienie odpowiedniego poziomu leczenia dzięki wystarczającej liczbie łóżek na oddziałach intensywnej terapii.
Regiony mają wskazać właściwe rozwiązania organizacyjne, które pozwolą stawić czoła możliwemu wzrostowi potrzeb hospitalizacji w tym zakresie.
Niezależnie od tego, że każdy Region musi wskazać jako priorytetową jedną lub kilka struktur/budynków przeznaczonych wyłącznie do leczenia pacjentów z COVID-19 („COVID Hospital”) w zależności od dynamiki epidemiologicznej, trzeba też przygotować planowanie względem każdego obszaru, które przewidywałoby:
- wyodrębnienie w każdej strukturze szpitalnej miejsc odizolowanych, pozwalających na obserwację pacjentów sztucznie wentylowanych/wymagających intensywnej terapii z podejrzeniem infekcji SARS – Cov 2 – w oczekiwaniu na definitywny wynik testów diagnostycznych
- utworzenie miejsc wieloosobowej intensywnej terapii (przy fizycznym oddzieleniu od innych jednostek intensywnej terapii obecnych w szpitalu) przeznaczonych na hospitalizację i leczenie pacjentów zarażonych COVID- 19. Takie jednostki intensywnej terapii mają być tworzone priorytetowo w strukturach szpitalnych posiadających oddziały chorób zakaźnych i w szpitalach referencyjnych ECMO (w ramach działań przewidzianych przy tworzeniu sieci krajowej RESPIRA).
- sporządzenie protokołów wskazujących kryteria dostępu do intensywnej terapii pacjentów chorych na COVID 19, ich leczenia klinicznego i opieki nad nimi, dotyczących także dystrybucji i wykorzystania środków ochrony osobistej i odpowiedniego szkolenia personelu.
- przewidywanie zwiększenia pojemności każdej struktury szpitalnej poprzez wykorzystanie łóżek w strefie krytycznej obecnie niewykorzystywanych i/lub procedury mające na celu reorganizację zaplanowanej działalności;
- pilne planowanie kształcenia personelu medycznego przeznaczonego do używania systemów wentylacji i poprawnego korzystania ze środków ochrony osobistej.
Konieczne jest uruchomienie „systemu monitorowania ilości łóżek w strefie krytycznej” na poziomie regionalnym, do wykonania przez lokalne Centrum Powiadamiania Ratunkowego 118 (chodzi o numer alarmowy, w Polsce 112 – przyp. tłum.) aby zapewnić na bieżąco także monitorowanie ilości łóżek wieloosobowej intensywnej terapii, o czym była mowa w poprzednich punktach.
Wszystkie prośby o miejsca – łóżka w strefie krytycznej na intensywnej terapii dla pacjentów chorych na COVID 19, po ocenie przez lekarza anestezjologa, będą musiały być kierowane do Centrum Ratunkowego 118.
Centrum Ratunkowe 118 przystąpi do przenosin [zapewne chodzi o przenosiny chorych do szpitali, w których są wolne łóżka – przyp. tłum.], dostarczając środka i personelu odpowiednio wyszkolonego.
Każdy Region winien przekazać Ministerstwu Zdrowia, Generalnej Dyrekcji Planowania, w czasie do 48 godzin od otrzymania niniejszego okólnika, poprzez uwierzytelniony e-mail, następujące informacje:
- ilość łóżek na intensywnej terapii, gdzie będzie możliwa obserwacja pacjentów oczekujących na wynik testu;
- ilość łóżek na intensywnej terapii, oddalonych od siebie, z dostępem do próżni;
- datę możliwego uruchomienia każdej poszczególnej wieloosobowej intensywnej terapii;
- łączną ilość łóżek każdej poszczególnej wieloosobowej intensywnej terapii;
- ilość poszczególnych łóżek każdej poszczególnej wieloosobowej intensywnej terapii;
- ilość łóżek na oddziale chorób płuc i oddziale intensywnego nadzoru oddechowego;
- ilość łóżek w izolatkach na oddziale zakaźnym;
- zapotrzebowanie w aparaturę do monitorowania i do wentylacji inwazyjnej i nieinwazyjnej;
- pilne planowanie kształcenia personelu medycznego przeznaczonego do obsługi systemów wentylacji i poprawnego korzystania ze środków ochrony osobistej, do jak najszybszej realizacji, nie później niż w ciągu 5 dni.
Z danych obecnie dostępnych obraz choroby COVID 19 u pacjentów pediatrycznych wydaje się łagodniejszy. Jednakże pacjenci pediatryczni z potwierdzonym zakażeniem COVID 19, wymagający intensywnej opieki noworodkowej czy pediatrycznej, będą zebrani w strukturach szpitalnych wyznaczonych do tego celu przez Regiony, zgłoszonych do Ministerstwa równocześnie z wyżej wymienionymi informacjami.
Wskazówki dotyczące opieki nad dorosłym pacjentem w stanie krytycznym
- zacząć od 5L/min 02 utrzymując przepływ, aby osiągnąć saturację Sp02 ≥ 90% u osoby dorosłej i Sp02 ≥ 92-95% u kobiet w ciąży,
- wszystkie strefy przeznaczone dla pacjentów zarażonych przez SARI razem z COVID 19 muszą być wyposażone w pulsoksymetry, zestawy do tlenoterapii (kaniule nosowe, maski, maski z workiem) i nieinwazyjny monitoring elektrokardiograficzny oraz ciśnienia krwi,
- jest konieczne stałe monitorowanie parametrów życiowych, aby szybko zauważyć postępujące pogorszenie mogące prowadzić do zespołów septycznych i ARDS,
- mieć na względzie podstawowe choroby pacjenta, aby dostosować terapię i oceniać rokowania.
Podstawowe leczenie kliniczne pacjenta z hipoksemią i niewydolnością oddechową
U pacjenta z ostrą hipoksemią może występować uporczywa duszność pomimo przepływów tlenu >10-15L/min, przez maskę z workiem. W takich przypadkach mogą być użyteczne High-flownasaloxygen (HFNO) lub wentylacja nieinwazyjna (NIV) do zastosowania po umieszczeniu pacjentów w odpowiednich strukturach szpitala.
Ponadto jest konieczne dodanie kolejnych łóżek w strefie krytycznej, a także wykorzystanie ewentualnych łóżek dotąd niewykorzystanych lub reorganizacja zaplanowanych działań. Jest ważne, by uwzględniać wysokie ryzyko niepowodzenia i konieczność uważnego monitorowania, gdyż może dojść do pogorszenia, nawet gwałtownego, stanu klinicznego.
Nie ma definitywnych wytycznych co do zastosowania wentylacji nieinwazyjnej u pacjenta z hipoksemią, jednak tam, gdzie narzuca się konieczność zastosowania takich technik, trzeba mieć na względzie możliwość szybkiego pogłębienia hipoksemii. Uwzględniając ryzyko niepowodzenia wentylacji nieinwazyjnej, jest konieczne leczenie takich pacjentów mając bezpośrednio do dyspozycji personel zdolny do przeprowadzenia intubacji dotchawiczej.
Zastosowanie wentylacji nieinwazyjnej może dokonywać się na różne sposoby w zależności od możliwości i wskazań (maska na usta-nos, total face lub hełm). Przy wyborze zastosowania wentylacji nieinwazyjnej trzeba też uwzględnić potencjalną dyfuzję cząstek aerozolu w otoczeniu.
W przypadku niepowodzenia wentylacji nieinwazyjnej i zastosowania intubacji dotchawiczej należy dokonać preoksygenacji za pomocą 100% FiO2 przez maskę twarzową, maskę z workiem, HFNO lub wentylację nieinwazyjną.
Pacjenci z niestabilnością hemodynamiczną lub niewydolnością wielonarządową albo zaburzeniem stanu umysłowego nie powinni być leczeni metodą wentylacji nieinwazyjnej.
Sekwencja szybkiej intubacji jest wskazana z uwzględnieniem ryzyka trudnych dróg oddechowych (Załącznik 1).
Wszystkie przytoczone procedury muszą być przeprowadzane przez pracowników odpowiednio wyszkolonych, używających środków ochrony osobistej do różnych procedur odpowiednio do ryzyka kontaktu z czynnikiem zakaźnym w otoczeniu.
Wskazówki proceduralne w leczeniu pacjenta z ARDS
Kiedy pacjent potrzebuje intubacji dotchawiczej, radzi się uwzględnienie algorytmu przytoczonego w załączniku 1.
Zastosować wentylację mechaniczną ochronną stosując niskie objętości oddechowe (4-8 ml/kg predicted body weight, PBW) i ciśnienia plateau ≤26-28 cmH20 przy drivingpressure (ciśnienie plateau- PEEP) ≤12-14 cm H20.
Radzi się zastosowanie blokerów przewodnictwa nerwowo-mieśniowego w pierwszych 24 godzinach od rozpoczęcia wentylacji mechanicznej u pacjentów z poważnym ARDS.
Gdyby wentylacja mechaniczna nie przyniosła polepszenia wymiany gazowej i PaO2/FiO2 byłaby poniżej 150, ułożyć pacjenta na brzuchu na przynajmniej 16 godzin. U pacjentów z ARDS umiarkowanym lub ciężkim jest możliwe zastosowanie wyższych wartości PEEP.
Orientacyjnie radzi się stosowanie następujących tabel kombinacji PEEP/FiO2:
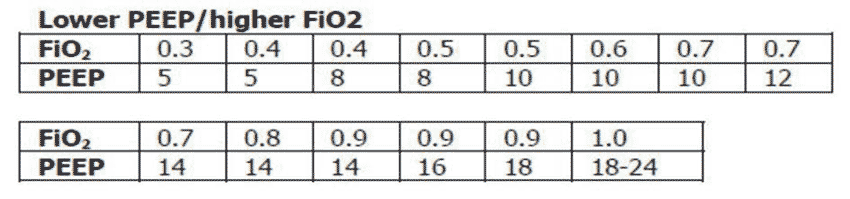
dążąc do uzyskania następujących celów terapeutycznych:
- SpO2 88‐95%
- PaO2 55‐80 mmHg
- PPLAT ≤ 26 cmH2O, ≤ 28 cmH2O jeśli BMI > 30
- DRIVING PRESSURE ≤ 12
Nie ma definitywnych wytycznych co do zastosowania ciągłego pozaustrojowego natleniania krwi (ECMO) u pacjentów z PaO2/FiO2 < 100mmHg.
W razie potrzeby zastosowania ECMO zaleca się centralizację pacjentów w ośrodkach z dostatecznym doświadczeniem, zwłaszcza należących do sieci RESPIRA.
Podczas wentylacji mechanicznej jest ważne unikanie odłączenia pacjenta od respiratora, co groziłoby derekrutacją, gwałtownym spadkiem ciśnienia dróg oddechowych i wysokim ryzykiem dyfuzji cząstek aerozolu w otoczeniu. W tym celu konieczne jest stosowanie zamkniętych systemów ssących.
Gdyby brakowało łóżek na intensywnej terapii dla pacjentów, których trzeba poddać sztucznej wentylacji wspomaganej, trzeba pilnie przeorganizować zaplanowane działania chirurgiczne, wykorzystując sale operacyjne i ich wyszkolony personel, jak również obecne tam urządzenia.
Alternatywnie można rozważyć następujące opcje umieszczenia pacjentów:
- jednostki intensywnego nadzoru oddechowego oddziałach chorób płuc, wykorzystując personel wyszkolony w procedurach oddechowych i przeznaczony do nich, jak też obecne tam urządzenia;
- jednostki chorób zakaźnych dysponujące poziomami izolacji, wykorzystując personel, który został wyszkolony w procedurach kontroli infekcji, ale będzie musiał być wyszkolony do zastosowania urządzeń do wspomagania oddychania. Te urządzenia trzeba będzie nabyć.
Dodatek – kryteria dla ARDS
Łagodne ARDS: 200 mmHg < PaO2/FiO2 ≤ 300 mmHg, przy PEEP albo CPAP ≥5 cmH2O, lub nie wentylowanych.
Umiarkowane ARDS: 100 mmHg < PaO2/FiO2 ≤200 mmHg przy PEEP ≥5 cmH2O lub nie wentylowanych.
Poważne ARDS: PaO2/FiO2 ≤ 100 mmHg przy PEEP ≥5 cmH2O lub nie wentylowanych.
Kiedy nie ma się do dyspozycji PaO2, SpO2/FiO2 ≤315 sugeruje obecność ARDS (włącznie z pacjentami nie wentylowanymi).
BIBLIOGRAFIA
ARDS Definition Task Force, Ranieri VM, Rubenfeld GD, et al. Acute respiratory distress syndrome: the Berlin Definition. JAMA 2012;307:2526‐33.
Riviello ED, Kiviri W, Twagirumugabe T, et al. Hospital Incidence and Outcomes of the Acute.
Respiratory Distress Syndrome Using the Kigali Modification of the Berlin Definition. Am J Respir.
Crit Care Med 2016;193:52‐9.
Rekomendacje WHO dotyczące SARI COVID-19.
Grupa ekspertów
Prof. Massimo Antonelli
Prof. Luca Richeldi
Prof. Roberto Bernabei
Prof. Alberto Villani






